베르베린 [Berberine] 항암·항균, 당뇨병 치료
천연항암물질 2014. 12. 16. 01:37 |베르베린 [Berberine] 항암·항균·항당뇨
암팔라야(Bitter Melon, 여주), 황련 뿌리(Coptidis Rhizoma), 매발톱나무 뿌리(Berberis vulgaris) 등에서 추출되는 이소퀴놀린 알칼로이드의 한 종류이다.
화학식 C20H19NO5·5H2O. 노란색 바늘 모양 결정이며 녹는점 145℃이다. 뜨거운 물이나 에탄올에는 잘 녹고, 클로로폼·벤젠에는 잘 녹지 않고, 에테르에는 녹지 않는다.
쓴맛이 나므로 황련과 황벽나무는 건위(健胃)·강장제·지사제(심한설사)·간해독제 등으로 중국과 인도 등지에서 수 세기 동안 쓰여왔다. 황련의 뿌리에서 약 4.1~7.4%의 베르베린을 추출할 수 있으며 암팔라야 말린 잎에서 5.6~8% 추출이 가능하다.
최근의 연구에서는 베르베린이 다양한 암종, 당뇨, 심장쇼크, 부정맥, 고혈압, 간독성, 알츠하이머 등에 탁월한 치료효과가 있는 것으로 밝혀졌다. (아래 참고자료)·
베르베린이 암세포 효소증식을 억제하여 암세포를 억제하고 면역증가 효과다 있는 것으로 연구 결과 나타났으며, 최근 한국, 중국, 호주의 과학자들이 공동으로 진행한 연구에 의하면 제2형 당뇨병과 비만에도 효과가 입증되었다.
연구결과 나타난 베르베린의 효능 Medical Benefits
질병치료 | 작용 메커니즘 |
항암작용 | ① 아데노심일인산(AMPK) 활성화로 세포주기 G1~M 단계에서 암세포의 성장과 증식을 억제한다.
② 암촉진 유전자[NF-kB, COX-2, PGE-2, TNF-a, IL-1b, IL-6, Bcl-2, cyclin, Bcl-XL, TNFα, MMPs, VEGF]의 활성을 억제하여 암세포의 성장과 증식, 전이를 원천봉쇄하였다.
③ 백혈병, 간암, 유방암, 피부암, 대장암, 전립선암, 갑상선암, 신경아종, 위암 등 대부분의 암종의 성장 억제효과를 발휘한다. |
항균작용 | 콜레라균(cholera), 대장균(Escherichia coli), rufgorrbs(Mycobacterium Tuberculosis), 헬리코박터파일로리균(Helicobacter Pylori), 칸디나균(Candida albicans), 이질균(Shigella dysenteriae), 살모넬라균(Salmonella ParatyPhi), 다양한 병원성이질균(Klebsiella sPecies)의 장 감염을 차단 |
당뇨병 치료 | ① 혈중 글루코스 감소 : 아데노산일인산효소(AMPK)을 자극하여 지방전구세포와 글루코스를 빨아들여 체중과 혈당이 빠른 속도로 현저히 감소하였으며 동시에 글루코스에 대한 내성을 완화시킨다.
② 인슐린 저항성 개선 : 인슐린수용체(InsR)의 발현을 증가시킴으로써 제2형 당뇨병 환자의 인슐린 저항성을 개선한다.
③ 췌장의 베타세포 자극 : 인슐린 분비를 촉진함으로써 항산화 기능이 강화되어 설령 글루코스 양이 늘어나더라도 이것이 산화되어 혈관벽에 쌓이는 것을 막아주고 동시에 지질을 적절히 분해함으로써 비만을 억제한다.
|
비만 해소 | 아데노산일인산효소(AMPK)을 자극, 비만을 일으키는 지방세포의 미토콘드리아 호흡사슬 복합체를 억제함으로써 산소 의존적인 글루코스의 산화를 감소시켜 비만을 해소한다. |
위장장애 개선 | 위장에서 간으로부터 담즙분비를 촉진하고 빌리루빈을 감소시켜 위장장애 해소 및 소화촉진 작용을 한다. |
간 보호 | ① 생체 내의 자연 항산화효소로 활성산소를 제거하는 SOD 및 카탈라제, GPX의 활성을 높여준다.
② 활성산소에 의한 조직손상이나 지질과산화 정도를 나타내 주는 GSSG 수치가 낮춰준다. |
심혈관질환 개선 | ① 혈관확장작용/항혈소판 작용을 통해 고혈압, 고지혈증, 부정맥, 동맥경화증을 개선한다. 베르베린의 혈관확장 효과는 아데노산일인산효소(AMPK)의 활성화를 통해 혈관내피확장효소(eNOS)를 발현시켜 산화질소(NO)의 생산을 증가시키는 것이다.
② LDL콜레스테롤을 제거함으로써 염증을 확대하는 유전자 [NF-B, Bcl-2, TNF-α, IL1ß] 및 혈관내피부착분자(ICAM-1)의 활성을 차단함으로써 심장병을 예방한다. |
뇌기능 개선 | ① 산화스트레스로부터 뇌세포를 보호함으로써 알츠하이머를 치료한다.
② 뇌세포 손상 복구로 기억력 개선 및 우울증을 치료한다. |
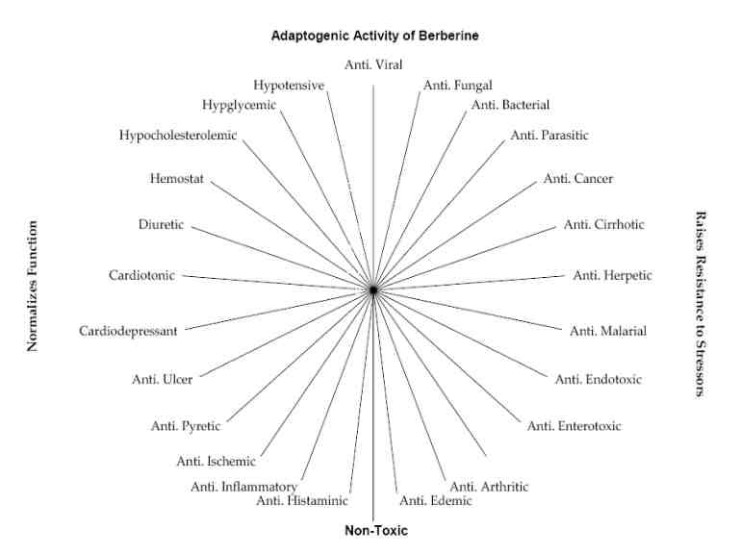
01. 베르베린의 항암작용 Anticancer
베르베린의 강점은 다양한 표적을 대상으로 항암효과를 낸다는 것이다. 미토콘드리아, DNA topoisomerases(DNA의 꼬인 가닥을 풀어주는 효소), 에스트로겐 수용체(estrogen receptor), MMPs(matrix metalloproteinase : 금속단백질 분해효소), p53, NF-kB 등 암세포의 성장에 관여하는 다양한 유전자들을 대상으로 활성억제 작용을 한다.
01. 베르베린의 항암 메커니즘
① 세포주기 차단

암치료에 있어 세포주기 차단은 일반적인 목표가 된다. 베르베린은 흑색종세포주(K1735-M2, WM793)에서 12.5~50 μM의 낮은 농도로 세포주기의 G1단계를 차단하며 50μM의 농도로는 G2단계를 차단하는 것으로 연구결과 나타났다.
더군다나, 폐암세포주(H1299, A549)에서는 베르베린 50 μM 농도에서 cyclin B1의 수준을 감소시키고 세포주기의 G1 단계를 차단함으로써 세포자살을 일으키는 것으로 나타났다.
프로그램화된 세포자연사(anokis)에 저항하는 유방암 세포주(MDA-MB-231 , MCF-7)에서는 베르베린 10~20μM 투여로 세포주기의 G0/G1 단계를 차단함으로써 5~10 μM을 투여한 항암제 독소루비신(doxorubicine)보다 암세포를 죽이는 능력이 뛰어난 것으로 드러났다.
② 암세포 성장경로 봉쇄
유방암세포주(MCF-7), 다형성아교모세포종(T98G), 구강암세포주(squamous carcinoma cancer-4 )에서 베르베린은 ① 종양억제유전자 카스파제-3 활성화를 통해 종양성장인자인 Bcl-2를 하향조절하고 억제인자인 Bax 및 p53 활성화 ⇒ ② 중합효소인 폴리머라제(polymerase)를 차단 ⇒ ③ 미토콘드리아에 의존하는 암세포 성장경로를 봉쇄 ⇒ ④ 세포자멸사를 유도하였다.
③ 자가포식에 의한 암세포 사멸
베르베린에 의한 또다른 세포자살 메커니즘은 암세포의 자가포식(autophagy)에 의한 것이다. 자가포식이란, 아폽토시스(apoptosis)와는 다른 형태의 세포사멸 방법으로 정상세포에서 낡고 쓸모없는, 수명을 다한 세포가 스스로를 집어삼켜 죽음을 선택하는 것이다.
간암세포주(HepG2, MHCC97-L)와 폐암세포주(A-549)에서 베르베린은 ① 종양억제유전자 베클린-1(beclin-1)을 활성화시키고 종양성장유전자 m-TOR의 활성을 억제 ⇒ ② 세포사멸 저해인자로 작용하는 3-메틸아데닌(3-methyladenine)을 제거 ⇒ ③ 암세포의 자가포식을 유도하였다.
④ 암세포의 대사작용 차단으로 전이 봉쇄
흑색피부종세포주(A375, Hs294)에서 베르베린은 종양촉진유전자 NF-kB의 활성을 억제하여 염증매개유전자인 프로스타글란딘(prostaglandin )을 차단함으로써 암세포의 침습을 봉쇄하였다. 프로스타글란딘은 염증을 확산시켜 암세포가 더욱 커지게 하고 침습을 일으키게 하는 중요한 효소로 작용한다.
상피세포암(HONE1 cells), 골수세포종(myelocytomatosis)에서 베르베린은 10 μM의 농도로 ① 암세포의 증식을 유도하는 효소인 GTPase의 활성을 억제하였으며 ⇒ ② 혈관신생유전자로 작용하는 금속단백질분해효소(MMP-9, MMP-2)와 혈관내피성장인자(VEGF)의 활성을 억제 ⇒ ③ 암세포가 새로운 혈관을 만들어 전이를 일으키는 것을 봉쇄하였다.
⑤ 복합처방으로 다재내성 암세포 사멸
베르베린은 항암제로 쓰이는 시스플라틴과의 복합처방으로 유방암세포주(HeLa, SH-SY5Y)에서 항암제를 단독사용할 때에 비하여 약물 민감성을 높여 세포사멸에 시너지효과를 발휘하였다.
간암세포주(HepG2)에서는 감마방사선치료시에 베르베린을 복합처방함으로써 방사선에 내성이 생긴 암세포의 세포자살효과를 현저하게 높여주었다. 골수성백혈병(lymphoblastic leukemia cells)에서는 기존 항암제에 저항성을 가진 다재내성 암세포를 효과적으로 제어하였다.
u 관련논문 : 천연 항암제 베르베린. Anti-cancer natural products isolated from chinese medicinal herbs
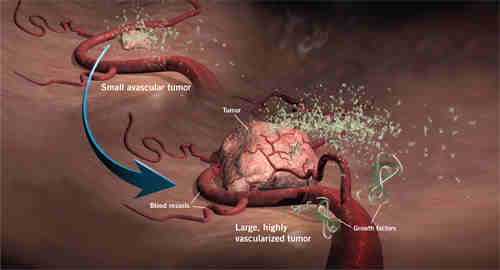
02. 혈관내피 손상과 동맥경화증
EFFECTS ON ENDOTHELIUM AND THE HEART
혈관 내피세포의 기능장애는 동맥경화증을 비롯하여 고혈압, 고지혈증, 당뇨병, 심부전증 등 심혈관질환의 중요한 요인이다.
특히 내피세포의 손상은 염증 반응과 함께 섬유화 증식을 초래하여 일련의 동맥경화증을 발생 또는 악화시킨다고 알려져 있다.

내피세포 기능장애는 활성산소로 인한 산화적 스트레스 (oxidative stress)와 산화 LDL콜레스테롤에 의하여 발생된다. 혈관벽의 LDL콜레스테롤은 마크로파지(대식세포)를 끌어들이고, 마크로파지는 다시 LDL콜레스테롤을 탐식하여 거품세포를형성한다. 이 과정에서 혈관내피부착분자(ICAM-1)의 혈중농도와 내피세포 기능장애는 상관관계를 보인다.
내피세포 기능장애는 여러 측면에서 그 병적 증상이 나타난다.
① 내피세포 의존성의 혈관 확장 (flow mediated dilatation: FMD) 장애
② 혈중 산화질소(NO) 농도의 감소 : 심부전 등에서 L-아르기닌 대사 이상으로 NO 합성의 감소.
③ 혈중 단백질 호르몬 엔도텔린(Endothelin) 수치 상승으로 인한 혈관 수축 증가
④ 내인성 ADMA(비대칭 다이메틸아르기닌)의 증가 : 고지혈증 환자에서 LDL콜레스테롤이 ADMA 합성을 증가시키고 파괴를 저해 시킴
⑤ 고지혈증시 활성 산소의 증가로 인한 산화질소(NO) 활성화의 억제. 활성 산소의 증가는 LDL콜레스테롤에 의한 L-아르기닌의 감소, 이로 인하여 NO 합성 장애가 있으며, 또한 관동맥 질환의 경우 항산화제(SOD) 활성도 감소로 인하여 활성 산소의 증가를 초래한다.
⑥ 염증 반응을 초래하는 감염이 발생하면 내피세포 기능장애를 초래할 수 있으며 클라미디아 균주나 살모넬라 백신 등에 의하여 발생할 수 있다.
베르베린의 동맥경화증 치료 메커니즘
연구결과에 따르면, 베르베린이 혈관내피(endothelium)세포와 그 아래에 있는 혈관민무늬근세포(vascular smooth muscle cell)에서의 이완작용을 함으로써 동맥경화증을 완화해주는 것으로 밝혀졌다.
작용기전 : 베르베린의 혈관확장 효과는 아데노산일인산효소(AMPK)의 활성화를 통해 혈관내피확장효소(eNOS)를 발현시켜 산화질소(NO)의 생산을 증가시키는 것이다.
게다가 베르베린은 혈관 내에 글루코스와 지방을 축적시키는 비만을 해소하는 작용을 포함해 내피세포에서 고혈당을 일으키는 다양한 부정적인 작용을 억제하였다.
또한 LDL콜레스테롤을 제거함으로써 염증을 확대하는 유전자 [NF-B, Bcl-2, TNF-α, IL1ß] 및 혈관내피부착분자(ICAM-1)의 활성을 차단하는 것이 확인되었다.
결과적으로, 산화질소(NO) 생성을 늘려 혈관확장을 유도함으로써 혈관내피세포의 손상을 치료하고, 그 결과로 동맥경화증을 개선, 비만요소를 제거, 당뇨 개선하는 효과를 가져왔으며, 염증 유발 유전자를 차단하여 궁극적으로 심혈관질환의 확대를 원천 봉쇄하였다.
u 관련논문 : 베르베린, 심장혈관과 대사작용 효과 Cardiovascular and metabolic effects of Berberine
03. 베르베린의 간 보호작용
Hepatoprotective effects of berberine
동물의 노화 원인은 방사선이나 자외선에 장시간 노출되거나 중금속 등에 의한 체내 오염, 합성약물의 남용 그리고 과도한 물리적, 정신적 스트레스 등을 받게 되면 생체내의 생화학적 반응에 의하여 자유라디칼(free radical)이 생성되고 이 자유라디칼들에 의하여 세포나 조직이 구조적, 기계적 손상을 받아 노화가 촉진되는 것이다. .
생명체는 독성에 의한 조직손상으로 부터의 보호를 위한 방어체계를 갖추고 있다. SOD, 카탈라제, GPX 등과 같은 내인성 항산화 효소나, 글루타치온과 같은 항산화 물질들이 조직 내에서 생성되는 자유라디칼들을 포착 제거할 수 있다고 알려져 있다.
이와 같은 생체내 방어기구에 이상이 초래되거나 각종 물리적, 화학적 요인들에 의하여 활성산소의 생성이 생체 방어계의 용량을 초과하게될 경우 생명체는 산화에 의한 조직손상을 당하게 된다.
따라서 이와 같은 활성산소를 소거할수있는 화합물 또는 과산화물 생성을억제하는 항산화 물질 및 항산화 효소의 생성을 촉진하고 자극할 수 있는 물질들에 대한 연구가 활발히 진행되어지고있다.
군산대학교에 화학과의 “파라쿼트 독성에 대한 베르베린의 항산화 효과”에 대한 연구결과를 발표했다.
제초제로 많이 이용되고 있는 파라쿼트(Paraquat)에 의해 간독성을 일으킨 생쥐에 베르베린을 1mg/kg/day 농도로 5일간 투여 후 관찰한 결과
① 생체 내의 자연 항산화효소로 활성산소를 제거하는 SOD 및 카탈라제, GPX의 활성을 높여주는 것으로 나타났으며
② 활성산소에 의한 조직손상이나 지질과산화 정도를 나타내 주는 GSSG 수치가 낮아진 것으로 나타났다.
③ 역시 생체 내에서 활성산소를 제거하고 세포를 보호하는 글루타치온의 활성이 증가되었다.
④ 활성산소와 세포막의 불포화지방산이 일련의 연쇄반응을 일으켜 발생하는 지질과산화의 최종 산물인 MDA 함량은 비타민 C와 비교해서도 현저하게 낮게 나타났다.
결과적으로 베르베린은 생체 내에서 강력한 항산화작용을 함으로써 독성 화학물에 중독된 간 조직의 세포를 보호해주는 효과가 있는 것으로 밝혀졌다.
u 관련논문 : 베르베린, 사염화탄소로 만성 간독성을 일으킨 마우스에서의 간 보호효과. Hepatoprotective effects of berberine on carbon tetrachloride-induced acute hepatotoxicity in rats
04. 베르베린과 류마티스 관절염
Effects of berberine on human rheumatoid arthritis
류마티스 관절염은 암의 형성과 유사한 확산 과정을 거친다. 즉, 염증으로부터 출발하여 활성산소의 지속적인 공격으로 면역시스템이 붕괴되고 면역세포와 전사단백질이 돌연변이를 일으켜 정상세포를 공격하고 염증을 확장시켜 나간다.
특히, 류마티스관절염에서는 활막세포(fibroblast-like synoviocytes)가 중요한 역할을 하는데, 빠른 속도로 감염을 확산시키고 감염된 세포의 자멸사를 방해한다.
연구결과, 세포주기의 G0/G1 단계에서 염증세포의 성장을 성장과 증식을 차단하는 것으로 밝혀졌다.
메커니즘 : ① 베르베린은 사이클린 의존성 효소(cyclin-dependent kinase : CDK)의 발현을 통해 염증촉진유전자 [Cip1/p21, Kip1/p27, CDK2, CDK4 , CDK6, cyclins D1, D2 , E] 활성을 억제하였으며,
② 이 과정에서 베르베린은 항아폽티스유전자[Bcl-2, Bcl-XL]의 발현을 막고 미토콘드리아 세포막의 방해, 억제유전자 [Bax, capase-의 활성을 촉진함으로써 활막세포의 사멸을 유도하였다.
u 관련논문 : 류마티스관절염에서의 베르베린의 효과. Effects of berberine on human rheumatoid arthritis fibroblast-like synoviocytes Abstract
05. 베르베린과 알츠하이머
Inhibitory Activities of Berberine in Alzheimer
역시 활성산소 공격으로 인한 뇌세포의 파괴로 생겨나는 알츠하이머는 노년층의 가장 공포스러운 질병이다.
기억력 상실, 행동장애 등으로 본인도 모르는 사이 가족들에게 커다란 정신적 고통을 가져다 주기 때문이다.
그런데, 이러한 사회적 질병을 치료할 마땅한 수단은 거의 없는 실정이다.
연구결과, 베르베린이 항산화작용을 포함하여 독성을 일으켜 뇌세포를 파괴하는 아세틸콜린 가수 분해 효소(acetylcholinesterase)와 부틸콜린가수분해효소(butyrylcholinesterase), 모노아민산화효소(monoamine oxidase)
아밀로이드 펩타이드(amyloid-b peptide) 등의 활성을 억제함으로써 세포 손상으로부터 회복, 기억력 회복에 효과가 있는 것으로 밝혀졌다.
u 관련논문 : 베르베린, 병원성효소 차단으로 알츠하이머 억제효과. Molecular Basis of Inhibitory Activities of Berberine against Pathogenic Enzymes in Alzheimer’s Disease
공급원 Source
암팔라야 잎(Bitter Melon : 5.6~8%), 황련 뿌리(Coptidis Rhizoma : 4.1~7.4%), 황벽나무 수피(Phellodendron amurense: 2~4%), Berberis aristata(4.2~5%), 매발톱나무뿌리(Berberis vulgaris : 0.4~1%)
Ø 추가 참고자료
① 알칼로이드 베르베린 광벙위한 약리활성직용. Berberine: Alkaloid with wide spectrum of pharmacological activities
② 베르베린, 간암세포주(HepG2)에서 침습억제. Berberine Inhibits Human Hepatoma Cell Invasion without Cytotoxicity in Healthy Hepatocytes
http://www.plosone.org/article/info%3Adoi%2F10.1371%2Fjournal.pone.0021416
③ 베르베린 흑색종세포주에서 COX-2, 프로스타글란딘 발현 억제로 암세포의 전이 차단. Berberine, an isoquinoline alkaloid, inhibits melanoma cancer cell migration by reducing the expressions of cyclooxygenase-2, prostaglandin E2 and prostaglandin E2 receptors
④ 베르베린, 위암세포주(SNU-5)에서 세포주기 차단. Berberine induces cell cycle arrest and apoptosis in human gastric carcinoma SNU-5 cell line
http://www.wjgnet.com/1007-9327/12/21.pdf
⑤ 베르베린, 갑상선암(8505C, TPC1) 성장 억제. Berberine Inhibited the Growth of Thyroid Cancer Cell Lines 8505C and TPC1
⑥ 베르베린, 유방암(MCF-7, MDA-MB-231) 성장억제. The alkaloid Berberine inhibits the growth of Anoikis-resistant MCF-7 and MDA-MB-231 breast cancer cell lines by inducing cell cycle arrest.
⑦ 베르베린, KCNQ1(심방세동을 일으키는 유전자) 채널 억제를 통해 대장암세포(T-84)에서 cAMP(사이클린의존성 아데노신 1인산염)유도 염화나트륨 분비 감소. Berberine Reduces cAMP-Induced Chloride Secretion in T84 Human Colonic Carcinoma Cells through Inhibition of Basolateral KCNQ1 Channels
⑧ 베르베린, 알츠하이머에서 병원성효소 억제작용. Molecular Basis of Inhibitory Activities of Berberine against Pathogenic Enzymes in Alzheimer’s Disease
⑨ 베르베린, 암세포 증식억제효과. ANTIPROLIFERATIVE ACTIVITY OF BERBERINE IN VITRO AND IN VIVO
'천연항암물질' 카테고리의 다른 글
| 엘라그산 Ellagic Acid (0) | 2015.03.06 |
|---|---|
| 캡사이신 [Capsaicin] 비만예방.암세포 억제 (0) | 2014.12.18 |
| 알칼로이드, 노스카핀 [Noscapine] 백혈병과 전림선암 치료 (0) | 2014.12.11 |
| 알칼로이드, 빈크리스틴(Vincristine)...백혈병 치료 (0) | 2014.12.04 |
| 트리고넬린(trigonelline )... 항발암성, 항당뇨효과 (0) | 2014.12.04 |










